1.国际经验借鉴
国际上细胞治疗技术是按照药品管理,必须严格进行一、二、三期临床试验。国际上多个发达国家和地区已经颁布了干细胞应用的相关法规。美国FDA颁布了用于全面管理HCT/P(Human Cell and Tissue based Products)生产过程的指导规范,即cGTP(current Good Tissue Products)。欧盟、日本和台湾地区也颁布了相应的法规。表1列出了美国、欧盟、日本和韩国细胞治疗政策法规及监管信息:
表1.美国、欧盟、日本和韩国细胞治疗政策法规
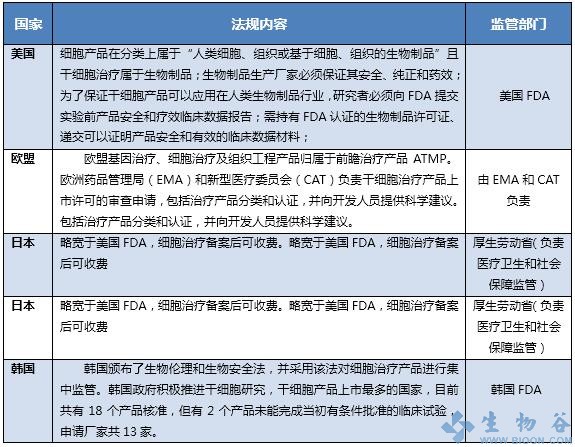
从上表可以了解到各国对细胞治疗的监管和相应的政策。
2.国外细胞治疗产品上市后的监管
目前全球已经批准一系列细胞治疗产品上市,干细胞治疗应用前景广阔,但现今大多数干细胞药物仍处在研发阶段。国际上已批准10多个干细胞药品上市,其中韩国的三种药物Hearticellgram-AMI、Cuepistem、Cartistem以及加拿大的Prochymal为干细胞药物,其余均为干细胞生物制剂。表2列出了目前已经上市的干细胞治疗产品:
表2已上市的干细胞产品
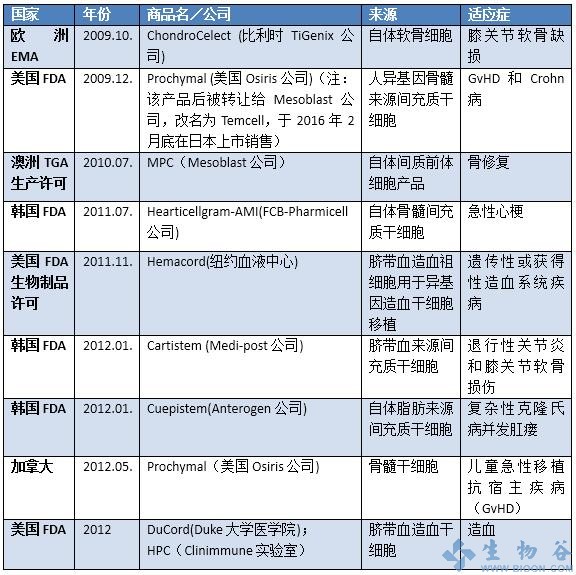
细胞治疗又分为免疫疗法和干细胞治疗,以干细胞为例,目前,在干细胞技术应用领域,美国、欧盟、日本、韩国等地的发展较为领先,相应的干细胞产品监管政策也较为完善,现对以上几个主要国家的干细胞产品的监管状况进行概述。
1).美国
美国食品药品监督管理局(FDA)把干细胞临床应用归类于细胞疗法。FDA负责保证生物制品的安全、纯度、效力和有效性,干细胞临床试验、干细胞治疗、干细胞产品生产、 销售等环节均由FDA下属的生物制品评估与研究中心(CBER)负责 监管。美国的干细胞产品审批过程和时间与其他生物制品药品一致, 但是具体审查的关注点可能会因产品而异[1]。 美国在干细胞治疗早期临床试验和监管方面有大量的经验, 其管理主要集中在3个基本方面[2]:①限制从捐赠者到接受者传染病传播的风险; ② 建立生产质量管理规范,使感染的风险降到最低; ③负责收集干细胞制品在加工过程中的安全性及有效性证明 。 目前,美国FDA正在努力与其他国家的监管部门探索国际干细胞治疗领域共同的管理制度,以求在全球干细胞产业进行统一监管,促进其安全、规范发展[3]。
2).欧盟
欧盟将干细胞产品归为新型治疗产品(ATMP),所有的干细胞产品均适用于新型医疗产品一样,评估需要210多天,由欧盟集中审查。在干细胞治疗应用的监管上,欧洲重视科学立法、政府引导、行业治理,实行行业管理机构之间无缝隙对接监管,提供必要的政府服务,使生物科技企业和医疗机构能够安全、科学、有效地研发干细胞产品[4]。欧盟于2004年颁布有关人体组织和细胞研究及应用的母指令(The Parent Directive),为成员国相关立法提供了一个制度框架[5];2006年颁布2个技术指令,为成员国相关立法提供了详细的技术基准,3个指令合称为细胞指令(EUTCD)。
欧盟各国成员均按照指令严格落实,以英国为例,在英国卫生体系(NHS)下,药品不能直接进入市场[6],英国在干细胞技术产品及药品监管上成立了人体组织管理局(HTA)及药品和保健产品监管署(MHRA)两个监管机构。HTA是由卫生部设立的具有执法和监管职能的非政府部门公共机构,规定干细胞基础研究和临床应用的各种标准,负责监督干细胞采集、处理、储存、分配以及患者的知情同意和临床治疗;MHRA是卫生部的执行机构,属于政府机构,负责监管干细胞产品的生产、加工、销售、评估及授权、不良反应监测,并根据不同的对象制定了一系列指南文件。HTA和MHRA规范有序的运作有效地确保了干细胞产品合理、安全的研发,积极推动了干细胞产业的发展[7]。欧盟表示,监管部门需谨慎平衡干细胞产品早期介入临床应用给患者带来的价值和无效药物的不良反应及其他风险的关系。研发商必须向监管部门提供与质量、安全和效力相关的证据,确保所有的药品安全、有效且质量优良等。
3).日本
在干细胞基础研究领域,日本政府从积极和长远的角度,在干细胞基础研究领域,日本政府从积极和长远的角度,在干细胞伦理、准则和社会应用等方面制定了有约束力的指导方针。日本卫生劳动福利部于2001年组织了干细胞临床研究专家委员会,集中讨论了干细胞技术临床应用的限制范围、临床评估系统、技术向临床转移以及其衍生产品的监管多个问题。2006年制定了关于干细胞应用安全和有效性的指导方针,以及对投资商和病人的伦理指导和知情同意制度,以确保治疗的安全、透明度以及隐私的保护。这两项指导确定了日本干细胞研究的双重评审系统[8]。
日本把干细胞临床试验分为疗效试验和临床研究2类,但日本的监管部门不参与临床研究,在一定程度上限制了其积累审查经验的机会[9]。在胚胎干细胞应用方面,日本成立了人类胚胎研究专家委员会,并制订了《人类胚胎干细胞研究准则》,规定日本各个协会的伦理委员会和国家的检查标准,每个伦理委员会通过的研究草案都要被详细地检查[10]。
4).韩国
在韩国,干细胞产品由韩国FDA进行监管,以确保产品的安全和有效性[11]。为了培育生命科学和生命技术,韩国颁布了生物伦理和生物安全法,并采用该法对干细胞产品进行集中监管[12]。该法案允许胚胎干细胞的研究,尤其支持成体干细胞的研究,同时也允许治疗性克隆,但禁止生殖性克隆和不同种族间精胚的转移。韩国国家生命伦理委员会对干细胞产品的类型、对象以及使用胚胎或人类胚胎干细胞的来源进行监管,国家卫生部部长提出具体审批意见[13]。韩国政府推出了关于推进干细胞产业投资发展的政策,通过立法来简化干细胞治疗产品授权的过程,减少干细胞产业化发展的障碍[14]。
二、国内法规政策:
1.相关政策规范
现如今,细胞治疗技术已经成为近年来最引人注目的领域之一,虽然国内细胞治疗研究不断取得重要成果,但仍存在一些会对细胞治疗技术的临床转化产生负面影响的不规范现象。为促进细胞治疗技术科学、有序地发展,几年来国家出台了一系列,以规范细胞治疗临床研究和应用行为的政策和法规。以下列出近年以来相关政策和法规:

2016年5月魏则西事件之后,5月4日,国家卫生计生委召开了关于规范医疗机构科室管理和医疗技术管理工作的电视电话会议,会议重申,自体免疫细胞治疗技术按照临床研究的相关规定执行。业界普遍认为,该规定进一步明确了国内免疫细胞治疗的行业标准,规范了临床应用,对推动整个行业的健康持续性发展具有重大意义。会议要求,各级卫生计生行政部门要立即组织对辖区内医疗机构违规出租或变相出租科室、违规开展医疗技术临床应用的情况开展全面清理,积极配合工商部门查处违法发布医疗广告的行为,以高度负责的态度,认真履职尽责,更好地维护人民群众的健康权益。
对于卫计委发布的新规,业内人士纷纷表示,新规明确了第三类医疗技术如进行临床应用必须要经过严格的审批,这就意味着缺乏核心技术、没有确实疗效的细胞免疫治疗技术将彻底被淘汰,这一举措实际上是提高了这个行业的准入门槛,将使一大批没有核心技术能力的公司退出市场,有利于结束目前国内免疫细胞治疗行业鱼龙混杂的局面。其次,此次监管部门监管的对象主要是指“基层医疗机构”,这为更多具备临床试验资质的机构、优秀公司创造了发展机会。
2.我国细胞治疗的监管之路
在我国,干细胞的伦理监管由国家卫生和计划生育委员会、科技部以及各医疗机构的伦理委员会负责;国家卫生和计划生育委员会和食品药品监督管理局负责干细胞治疗及产品的审批和监管。由上表中列出的细胞治疗政策法规和发展历程可了解到我国对细胞治疗的监管具体情况。魏则西事件之后国家卫计委重申了关于规范医疗机构科室管理和医疗技术管理工作的重要性,此举规范了临床应用,但是与国外相比,国内监管力度不够且对细胞治疗的明确的监管文件均为指南、原则等形式,还没有上升到法律层面。(生物谷Bioon.com)
参考文献
[1] Kellathur SN, Lou HX. Cell and tissue therapy regulation: worldwide status and harmonization [J]. Biologicals, 2012, 40 (3): 222-224.
[2] Future Science Group. European Medicines Angency, CAT Secretariat & US Food and Drug Administration [J]. Regen Med, 2011, 6(6 suppl): 90-96.
[3] Committee for Advanced Therapies. Challenges with advanced therapy medicinal products and how to meet them [J]. Nat Rev Drug Discov, 2010, 9(3): 195-201.
[4] 黄清华. 英国执行EUTCD的经验和启示---兼谈中国干细胞疗法监管科学框架[J]. 医学与法学, 2013, 5(4): 15-22.
[5] 黄清华. 细谈欧盟三个细胞指令[J]. 科技导报, 2013, 31(30): 11.
[6] 黄清华. 英国卫生体系基本法研究[J]. 法制研究, 2012, 1(8): 46-59.
[7] 黄清华. 英国执行欧盟细胞指令的经验和启示[J]. 时代法学, 2014, 12(1): 104-113.
[8] Kawakami M, Sipp D, Kato, K. Regulatory impacts on stem cell research in Japan[J]. Cell Stem Cell, 2010, 7(6): 415-418.
[9] 河野修己. 在亚洲推广的再生医疗即将进入建立制度阶段[J]. 生物产业技术, 2013, 1(3): 26-28.
[10] 位田隆一. 日本的人类胚胎干细胞研究[J]. 医学与哲学, 2004, 25(4): 15-17.
[11] Oh IH. Regulatory issues in stem cell therapeutics in Korea: efficacy or efficiency? [J]. Korean Hematol, 2012, 47(2): 87-89.
[12] 谢正福. 国内外干细胞研究及临床应用监管状况[J]. 生命的化学. 2013, 33(4): 478-482.
[13] Mi-Kyung Kim. Oversight framework overoocyte procurement for somatic cell nuclear transfer: comparative analysis of the Hwang Woo Suk case under South Korean bioethics law and U.S. guidelines for human embryonic stem research [J]. Theor Med Bioeth, 2009, 30(1):367-384.
[14] 姜天娇, 孙金海. 国外细胞产品监管现状及对我国的启示[J]. 中国社会医学杂志, 2016, 33(2): 117-122.